GIST 관련 소식란
악성 위장관기질종양의 진단 (진단코드 관련)
내용
진료현장에서 위장관기질종양의 진단에 있어, 특히 외과의 경우 “악성위장관기질종양”의 진단에 어려움이 있습니다. 보험사 및 환자의 이해관계 중간에 임상의가 어떤 근거에 입각하여 “악성위장관기질종양”이라 명명해야 하는지에 관해 우리나라 소화기병리학회에서 제안한 논문과 이를 요약하면 다음과 같습니다. 소화기종양의등록코드
- 논문제목 : 병리의사를 위한 소화기계 암등록에 대한 제안
- 논문의 취지 : 본 논문은 소화기병리학회에서 2008년 국내병리학자 240명을 대상으로 설문작업을 하여 ICD-O3라 는 현재 우리나라에서 사용되는 질병분류코드와 임상에서 잘 맞지 않아 어려움이 있는 부분을 어떻게 consensus를 만들어 임상의사에게 지침을 줄 것인지에 대한 가이드라인 입니다.
- 논문요약 : 본 논문에 따르면 GIST는 2002년 NIH분류법을 따르는 것으로 하고
1) 2002 NIH분류에 근거한 intermediate or high risk
2) 수술 과정 중 터졌거나 재발되어 수술한 환자
3) 진단 당시 원격전이가 있거나 주변 장기로의 침윤이 관찰되는 경우
Diagnosis_of_Gastrointestional_stromal_tumors_a_consensus_approach
를 악성으로 기술하였습니다. 그러므로 임상에서는 위 세가지 요건 중 하나에 해당되는 경우 “악성위장관기질종양”으로 진단할 수 있습니다.
- 연구회 의견
본 논문은 “악성위장관기질종양”의 진단에 있어 원발 부위에 대한 고려가 없다는 것(2002 NIH분류법)이 단점이지만, 병리과학회에서는 2008년도에 발표된 내용이므로 단시간 내에 개정할 계획은 없다고 합니다.
그러므로 병리과학회를 통해 새로운 근거논문이 나오기 전에는 위 세가지 요건에 입각하여 진단서를 작성하시기를 추천합니다.
GIST 보험관련 소식
구분
23. 연조직육종〔2군 항암제를 포함한 요법] 2010-5호공고전문
세부인정기준 및 방법
| 연번 | 항암화학요법 | 투여대상 | 투여단계 | 투여요법 |
|---|---|---|---|---|
| 1 | (GIST)imatinib mesylate | 나. 성인의 Kit(CD 117) 양성인 위장관기 질종양 환자로 다음의 조건을 모두 만족하는 경우 (투여인정기간 : 최초 투여 후 최대 1년) ① 근치적 절제술 후 종양의 증거가 없고 ② high risk 이상의 위험도 환자 | - | A |
※ 투여요법 : A(수술 후 보조요법, adjuvant)
주1. 연번 1-나 관련
(1) ‘수술 후 보조요법’으로 투여하는 경우 재발여부나 부작용 발생여부 등 3~6개월마다 평가하면서 투여하도록 함.
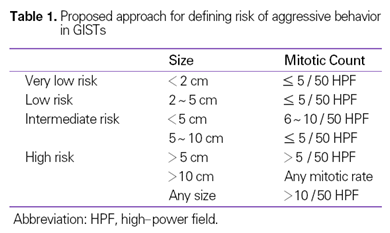
(2) Proposed approach for defining risk of aggressive behavior in GISTs
| Size | Mitotic count | |
|---|---|---|
| Very low risk | <2 cm | <5/50 HPF |
| Low risk | 2-5 cm | <5/50 HPF |
| Intermediate risk | <5 cm | 6-10/50 HPF |
| 5-10 cm | <5/50 HPF | |
| High risk | >5 cm | >5/50 HPF |
| >10 cm | Any mitotic rate | |
| Any size | >10/50 HPF |
(by NIH Consensus Meeting)
(시행일 : 2010.3.1)
사유
- imatinib mesylate(품명 : 글리벡필름코팅정 100mg)"이 <성인환자에서 Kit (CD 117) 양성 위장관 기질종양 절제 수술 후 보조요법>으로 새로이 허가가 추가되어, 교과서, 가이드라인, 임상논문 등을 면밀히 검토한 결과
- 위장관기질종양의 치료에 있어서 근치적 절제수술이 가장 중요하며, 수술적인 절제가 가능한 경우에도 그 재발률이 높은 실정임. 따라서, 허가임상논문을 통해 발표된 자료에 따르면 글리벡정이 위장관기질종양의 수술 후 1년 보조요법에서 1년 무재발 생존률(recurrence free survival)이 위약군에 비해 유의하게 향상된 결과를 보인 점(98% vs. 83% p<0.0001)등을 고려하여 재발율을 낮출것으로 기대되는 바, 동 요법을 급여 인정키로 함
- 다만, 허가임상논문에서 글리벡정의 투여기간은 1년이었으며, 2년이상 투여에 대한 임상연구가 현재 진행중이므로 1년 이상투여에 따른 치료효과를 알 수가 없음. 또한, 허가임상논문을 통해 종양의 크기가 10cm를 넘는 경우 동 약제 투여로 인한 이득이 가장 큰 것으로 보고됨에 따라 이를 고려해야 할 것임
- 이에, 오남용의 소지가 있을 수 있음을 감안하여 수술 후 보조요법 시 충분한 평가를 하면서 사용토록 하는 등을 고려하여 급여기준을 설정함
검토결과
- 식약청 허가사항이 추가됨에 따라 우리 원의 ‘암질환심의위원회’ 심의를 거쳐 설정된 급여기준을 공고하게 됨